Болезнь Паркинсона — хроническое прогрессирующее неврологическое заболевание. Заболевание поражает небольшую часть головного мозга, в которой производится большая часть дофамина. Дофамин — это химическое вещество, с помощью которого передаются сигналы между нервами, контролирующими мышечные движения, а также нервами, участвующими в других функциях организма. Отмирание клеток, вырабатывающих дофамин, в процессе старения считается нормой. Этот процесс происходит у большинства пациентов очень медленно, но у некоторых потеря происходит быстро, что является началом болезни Паркинсона.
Основные методы диагностики при болезни Паркинсона:
- Клиническое обследование позволяет выявить характерные двигательные нарушения, включая тремор покоя, ригидность, брадикинезию и постуральную нестабильность, а также оценить динамику симптомов и реакцию на дофаминергическую терапию. Неврологический осмотр включает выполнение тестов на координацию, тонус и ходьбу, что помогает дифференцировать болезнь Паркинсона от атипичных паркинсонизмов.
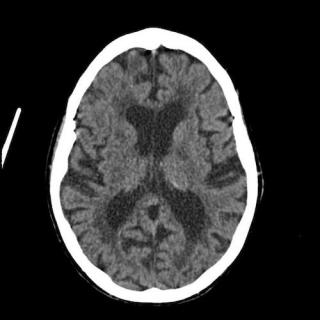
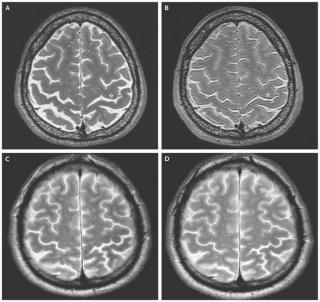
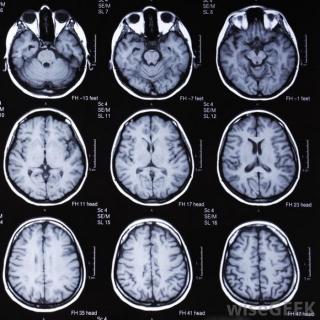
- Магнитно-резонансная томография головного мозга позволяет исключить сосудистый, посттравматический и опухолевый паркинсонизм, а также выявить атрофию черной субстанции и снижение объема базальных ганглиев. В режимах с подавлением сигнала от воды оценивается снижение интенсивности в зоне черного вещества, что коррелирует с выраженностью дегенеративных изменений.
- Функциональная нейровизуализация с использованием позитронно-эмиссионной томографии или однофотонной эмиссионной компьютерной томографии с дофаминергическими маркерами позволяет определить снижение накопления радиофармпрепарата в стриатуме, что свидетельствует о дефиците дофамина в нигростриарной системе.
- Транскраниальная сонография позволяет выявить гиперэхогенность черной субстанции, что указывает на повышенное содержание железа в этой зоне и коррелирует с нейродегенеративными изменениями. Метод применяется для ранней диагностики, особенно при наличии факторов риска болезни Паркинсона.
- Генетическое тестирование используется при подозрении на наследственные формы паркинсонизма, включая мутации в генах LRRK2, PARK2, SNCA, что особенно важно для пациентов с семейным анамнезом. Анализ полиморфизмов, ассоциированных с дофаминергической дисфункцией, может помочь оценить предрасположенность к заболеванию.
- Лабораторные исследования включают анализ крови на уровень меди и церулоплазмина для исключения болезни Вильсона, а также исследование уровня тиреоидных гормонов для выявления вторичных причин двигательных нарушений. Оценка уровня α-синуклеина в цереброспинальной жидкости проводится в исследовательских целях для выявления нейродегенеративных маркеров.
В большинстве случаев, МРТ головного мозга на томографе 3 Тесла и выше выбирается как первичный метод диагностики. Если результаты исследования носят тревожный или неясный характер, дополнительно назначается:
- Электроэнцефалография (ЭЭГ)
- Однофотонная эмиссионная компьютерная томография и Dopamine Transporter Scan
- Реоэнцефалография.
Призанки болезни Паркинсона
Болезнь Паркинсона прогрессирует, постепенно лишая пациента двигательных способностей. К основным симптомам заболевания относятся неуклюжая походка, ригидность конечностей, тремор и потеря равновесия.
Причины болезнь Паркинсона
Никто не знает, что вызывает болезнь Паркинсона. Большинство случаев возникают спонтанно; некоторые являются наследственными. Учеными выявлено, что когда от 50 до 60 % клеток головного мозга, производящие дофамин, отмирают, у пациента начинают развиваться симптомы болезни Паркинсона. Не существует биомаркеров или объективных скрининговых исследований, указывающих на наличие болезни Паркинсона. Тем не менее, медицинские эксперты показали, что с этим связано множество факторов. Чаще всего болезнь поражает пациентов в возрасте от 65 лет. Причины болезни Паркинсона, вероятно, связаны с генетикой, окружающей средой или другими неизвестными факторами. От 10 до 20 % случаев болезни Паркинсона связаны с генетической причиной. Типы бывают либо аутосомно-доминантными (при которых пациент получает одну копию мутировавшего гена от одного родителя), либо аутосомно-рецессивными (при котором наследуется копия мутировавшего гена от каждого из родителей). Но при этом большинство случаев болезни Паркинсона остаются идиопатическими, что означает отсутствие ясно выявленной причины.
Самым большим фактором риска развития болезни Паркинсона является преклонный возраст. Средний возраст начала — 60 лет. Мужчины более склонны к развитию болезни Паркинсона, чем женщины. Пациенты, у которых есть больные родители или братья и сестры, имеют риск развития болезни Паркинсона примерно в 2 раза выше
Медицинские эксперты считают, что факторы окружающей среды могут способствовать возникновению болезни Паркинсона. Воздействие сельскохозяйственных химикатов, таких как пестициды и гербициды; работа с тяжелыми металлами, моющими средствами и растворителями могут иметь связь с развитием заболевания с течением времени. Тем не менее маловероятно, что у большинства пациентов болезнь Паркинсона развивается из-за воздействия опасных факторов окружающей среды.
Повторяющиеся удары по голове увеличивают риск развития болезни Паркинсона.
Болезнь Паркинсона нечасто встречается у пациентов моложе 50 лет, но у небольшой группы больных болезнь проявляется рано. В редких случаях болезнь Паркинсона может быть диагностирована у пациентов моложе 40 лет — по текущим оценкам, около 2 % из 1 миллиона человек с болезнью Паркинсона были диагностированы в возрасте до 40 лет. Хотя больные, которым поставлен диагноз в молодом возрасте, сталкиваются с другим набором проблем, прогресс из заболевания намного легче.
Сложности диагностики болезни Паркинсона
Постановка точного диагноза болезни Паркинсона может быть затруднена. Невролог должен тщательно изучить симптомы, семейный анамнез и другие факторы, чтобы прийти к конкретному заключению. Стандартный диагноз болезни Паркинсона в настоящее время является клиническим. Это означает, что нет конкретного исследования , такого как анализ крови, МРТ, КТ, Электроэнцефалография, которое может дать окончательный результат. Вместо этого должны присутствовать определенные физические симптомы, чтобы квалифицировать состояние пациента как болезнь Паркинсона.
Поскольку не существует убедительного скрининга или исследования, пациенты с болезнью Паркинсона на очень ранней стадии могут не соответствовать критериям клинического диагноза. С другой стороны, это отсутствие специфичности означает, что у пациента может быть диагностировано другое заболевание, имитирующее болезнь Паркинсона.
На что обращают внимание врачи при диагностике болезни Паркинсона
Определенные физические симптомы, замеченные пациентом или его или ее близкими, обычно являются причиной обращения к врачу. Актуальны следующие сигнализирующие признаки:
- дрожь или тремор: так называемый тремор покоя, дрожание руки или ноги, которое обычно прекращается при выходе из состояния покоя
- брадикинезия: замедление движений конечностей, лица или тела в целом
- ригидность: скованность в руках, ногах или туловище
- нестабильность осанки: проблемы с балансом и возможные падения
Во время обследования пациента невролог:
- собирает анамнез и проводит медицинский осмотр
- выясняет список принимаемых препаратов. Некоторые лекарства могут вызывать симптомы, напоминающие болезнь Паркинсона
- проводит неврологическое обследование, проверяя ловкость, мышечный тонус, походку и равновесие.
МРТ, ЭЭГ или Реоэнцефалография при Болезни Паркинсона - что покажут
Не существует лабораторных или визуализирующих исследований, рекомендованных или определяющих болезнь Паркинсона. Врачи используют комплексные данные обследований, чтобыметодом исключения потаить диагноз - болезнь Паркинсона
- МРТ головного мозга при болезни Паркинсона хорошо показывают признаки вторичного паркинсонизма (сосудистый, посттравматический). Однако в случае паркинсонизма в рамках мультисистемных дегенераций МРТ далеко не всегда позволяет определить нейровизуализационные маркеры этих заболеваний. Особенно это имеет отношение к больным с продолжительностью заболевания до 1-2-х лет.
- Однофотонная эмиссионная компьютерная томография и Dopamine Transporter Scan. Этот метод позволяет врачам видеть подробные изображения дофаминовой системы мозга. DaTscan включает в себя инъекцию небольшого количества радиоактивного препарата и применение устройства, называемого сканером однофотонной эмиссионной компьютерной томографии (ОФЭКТ). Препарат связывается с передатчиками дофамина в головном мозге, показывая, где в головном мозге находятся дофаминергические нейроны. (Дофаминергические нейроны являются источником дофамина в мозгу; потеря дофамина — это то, что приводит к болезни Паркинсона.) Результаты DaTscan не могут точно выявить наличие болезни Паркинсона, но они позволяют врачу подтвердить диагноз или исключить имитацию болезни Паркинсона.
- Самой частой находкой в ЭЭГ больных паркинсонизмом является замедление основного ритма. Предполагалось, что замедление ритма может быть связано с возрастом. Однако у больных паркинсонизмом обнаружены более медленные ритмы, чем в контрольной группе того же возраста. В отдельных случаях отмечено полное исчезновение альфа-ритма в ЭЭГ больных.
- Реоэнцефалографией называют метод обследования центральной нервной системы и оценки церебрального кровоснабжения, основанный на разнице в электрическом сопротивлении крови, спинномозговой жидкости, головного мозга и других тканей. Данные РЭГ иногда используют для исключения сосудистых патологий.
Что хорошо покажет МРТ при болезни Паркинсона
- Глубина дегенеративных изменений в черной субстанции по степени снижения ее объема и четкости границ с окружающими структурами.
- Степень накопления железа в базальных ганглиях по изменению интенсивности сигнала в зоне бледного шара и полосатого тела.
- Атрофические изменения коры головного мозга по выраженности расширения борозд и желудочков, что отражает прогрессирование заболевания.
- Структурные изменения в нигростриарной системе по снижению контрастности между черной субстанцией и красным ядром.
- Микроструктурные нарушения в проводящих путях по снижению фракционной анизотропии в области среднего мозга.
МРТ при болезни Паркинсона выявляет следующие характерные признаки:
На Т1-взвешенных изображениях объем базальных ганглиев и черной субстанции может быть уменьшен, что свидетельствует об атрофических изменениях в нигростриарной системе.
На Т2-взвешенных изображениях снижение интенсивности сигнала в области черной субстанции проявляется как гипоинтенсивные участки, что связано с накоплением железа и дегенеративными процессами. Изменение плотности сигнала в области полосатого тела и бледного шара коррелирует с прогрессированием заболевания и потерей дофаминергических нейронов.
На изображениях с подавлением сигнала от воды четкая граница между черной субстанцией и красным ядром может отсутствовать, что указывает на структурные изменения и потерю нейронов. Отсутствие нормального гиперинтенсивного сигнала в зоне задней части черной субстанции свидетельствует о дегенерации нигростриарного пути.
На диффузионно-взвешенных изображениях снижение фракционной анизотропии в области среднего мозга отражает дегенерацию проводящих путей и нарушение микроструктурной организации тканей. Уменьшение диффузии в области базальных ганглиев может быть связано с прогрессирующей нейродегенерацией и утратой нейронов.
На функциональных МРТ-исследованиях изменение активности в области моторной коры и стриатума фиксируется в виде нарушения функциональных связей между этими зонами. Динамическая оценка кровотока в области базальных ганглиев показывает снижение перфузии, что свидетельствует о метаболических изменениях, характерных для болезни Паркинсона.
Оданко томография плохо визуализирует следующие аспекты патологии:
- Функциональное состояние базальных ганглиев и их активность, что исключает возможность анализа нейромедиаторных процессов.
- Циркуляторные изменения и нарушение кровотока в нигростриарном пути, что ограничивает оценку сосудистых факторов прогрессирования.
- Начальная стадия болезни без выраженной атрофии черной субстанции, что снижает точность диагностики на доклиническом этапе.
- Изменения в активности кортикальных и подкорковых сетей, что исключает возможность оценки динамики нарушений.
Что хорошо покажет ЭЭГ при болезни Паркинсона
- Степень замедления фоновой активности по снижению частоты и амплитуды альфа-ритма в затылочных и теменных областях.
- Нарушение корково-подкорковых связей по сниженной реактивности альфа-ритма на сенсорные стимулы и изменению его десинхронизации.
- Структурные изменения сенсомоторных ритмов по уменьшению мощности ритма в центральных зонах, что отражает снижение активности моторной коры.
- Функциональное состояние лобных долей по выраженности тета-активности, что коррелирует с когнитивными нарушениями.
- Изменение паттернов сна по снижению количества сигма-волн и уменьшению активности сигма-ритма, что свидетельствует о нарушении глубокой фазы сна.
ЭЭГ при болезни Паркинсона выявляет следующие характерные признаки:
Общее снижение амплитуды и частоты фоновой активности проявляется уменьшением мощности α-ритма и его замедлением, что свидетельствует о дисфункции корково-подкорковых связей. Доминирование медленной θ-активности фиксируется в лобных и центральных областях, что коррелирует с когнитивными нарушениями.
Нарушение сенсомоторного ритма проявляется снижением амплитуды μ-ритма в центральных зонах, что отражает ухудшение регуляции двигательной активности. Ослабление бетта-ритма в моторной коре свидетельствует о сниженной активности нейронов, участвующих в контроле движений.
Дисфункция подкорково-корковых сетей фиксируется по сниженной реактивности альфа-ритма на сенсорные стимулы, что указывает на нарушение функциональной связи между базальными ганглиями и корой. Асимметричность электрической активности в лобных и центральных зонах выявляется при прогрессировании болезни, что отражает постепенную потерю межполушарных связей.
Эпизодическая гиперсинхронизация активности в передних отделах мозга выявляется при выраженных когнитивных нарушениях, что коррелирует с развитием паркинсонических деменций. Уменьшение амплитуды реактивных потенциалов в ответ на внешние раздражители фиксируется при исследовании вызванных потенциалов, что свидетельствует о сниженной пластичности нервной системы.
Изменение паттернов сна характеризуется уменьшением фаз медленного сна и нарушением генерации сигма-волн, что отражает дисфункцию стволовых структур мозга. Уменьшение активности σ-ритма во время сна указывает на нарушение процессов консолидации памяти и ухудшение работы таламокортикальных цепей.
Оданко исследование плохо визуализирует следующие аспекты патологии:
- Морфологические изменения в черной субстанции и базальных ганглиях, что исключает возможность оценки их структурного состояния.
- Накопление железа в подкорковых структурах, что делает невозможным определение прогрессирования дегенеративного процесса.
- Функциональные изменения в дофаминергической системе, что ограничивает возможность оценки нейромедиаторных нарушений.
- Анатомические изменения в таламокортикальных цепях, что снижает точность диагностики ранних двигательных расстройств.
- Нарушение кровоснабжения в структурах среднего мозга, что исключает возможность оценки циркуляторных изменений.
Что хорошо покажет реоэнцефалография при болезни Паркинсона
- Степень снижения эластичности артериальных стенок по уменьшению крутизны восходящего колена реографической волны.
- Нарушение тонуса церебральных сосудов по снижению амплитуды реографической волны, что отражает ухудшение ауторегуляции кровотока.
- Величина асимметрии мозгового кровообращения по разнице реографических показателей между полушариями.
- Состояние венозного оттока по увеличению дикротического индекса, что указывает на застойные явления в венозной системе.
- Реакция сосудов на функциональные пробы по скорости изменения амплитуды реографической волны, что позволяет оценить адаптационные возможности кровотока.
Реоэнцефалография при болезни Паркинсона выявляет следующие характерные признаки:
Снижение тонуса церебральных сосудов определяется по уменьшению амплитуды реографической волны, что свидетельствует о гипотонии сосудистой стенки и нарушении ауторегуляции мозгового кровотока. Уменьшение эластичности артериальных стенок фиксируется по снижению крутизны восходящего колена реограммы, что отражает возрастные и дегенеративные изменения сосудов.
Нарушение венозного оттока визуализируется по увеличению дикротического индекса и изменению формы реографической волны, что свидетельствует о застойных явлениях в венозном русле. Дисбаланс между артериальным и венозным кровоснабжением выявляется по изменению времени полуспада пульсовой волны, что указывает на ухудшение дренажной функции вен головного мозга.
Снижение мозгового кровотока в лобных и теменных долях фиксируется по уменьшению кровенаполнения артериальных ветвей, что коррелирует с когнитивными нарушениями при прогрессировании заболевания. Асимметрия кровоснабжения в полушариях выявляется по разнице реографических показателей, что указывает на функциональные расстройства цереброваскулярной системы.
Нарушение реакции сосудов на функциональные пробы с гиперкапнией или ортостатической нагрузкой определяется по замедленной вазодилатации или недостаточному повышению амплитуды волны, что свидетельствует о сниженной компенсаторной способности церебральных артерий. Дефицит адаптационных механизмов кровотока фиксируется по замедленной нормализации реографических параметров после функциональной нагрузки.
Изменение периферического сопротивления сосудов оценивается по увеличению периферического реографического индекса, что указывает на спастические явления в церебральном кровообращении. Нарушение микроциркуляции в глубоких структурах мозга фиксируется по изменению формы анакротической части реограммы, что отражает ухудшение кровоснабжения базальных ганглиев.
Оданко сканирование плохо визуализирует следующие аспекты патологии:
- Морфологические изменения в структурах головного мозга, что исключает возможность оценки дегенеративных процессов в черной субстанции.
- Функциональное состояние нейронных сетей и проводящих путей, что делает невозможным анализ нейродинамических нарушений.
- Дегенеративные процессы в нигростриарной системе, что ограничивает точность диагностики болезни на ранних стадиях.
- Изменения циркуляции в глубоких структурах мозга, что снижает точность оценки кровотока в базальных ганглиях и среднем мозге.
Список медицинской литературы:
- Голубев В.Л., Левин Я.И., Вейн A.M. Болезнь Паркинсона и синдром паркинсонизма. М.: МЕДпресс, - 1999. - 416с.
- Крыжановский Г.Н., Карабань И.Н., Магаева C.B. и др. Болезнь Паркинсона: Этиология, патогенез, клиника, лечение, профилактика. М.: Медицина, 2002. 336 с.
- Левин О.С., Федорова Н.В. Болезнь Паркинсона. М.: Медпресс-информ; 2014. - С. 232-236.
- Левин О.С. Дифференциальная диагностика паркинсонизма / О.С. Левин, Н.В. Федорова, В.Н. Шток // Журн. неврологии и психиатрии. -2003. Т. 103, № 2. - С. 54-60.
- Федорова Н.В. Лечение болезни Паркинсона. // Русский медицинский журнал.-2001.-С. 24-33.
Обследование головного мозга - это сложная диагностическая задача для любого специалиста. Он надежно спрятан под черепными пластинами, поэтому в большинстве случаев доступен только для неинвазивных методов диагностики. В арсенале врачей есть следующие способы оценить различные аспекты анатомии и функции мозга:
Магнитно-резонансная томография позволяет визуализировать всевозможные участки человеческого тела и незаменима во многих случаях в диагностике неврологических заболеваний, а вот как часто можно делать МРТ, мы поговорим в этой статье. МРТ и МСКТ диагностика (компьютерная томография) - это разные по своим физическим принципам исследования.
В каких случаях врач должен назначить Вам МРТ головного мозга, а в каких ЭЭГ, и что из них лучше - обо всем этом подробнее мы поговорим в этой статье. Когда принимается решение о той или иной форме диагностики, доктор исходит из нескольких факторов: цель обследования и первичный диагноз;
 Служба бесплатной
Служба бесплатной