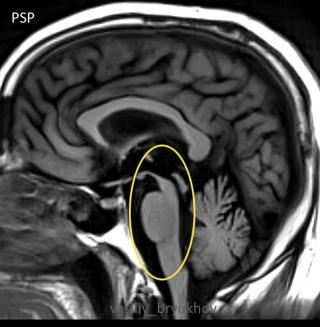
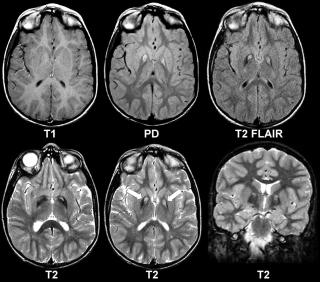
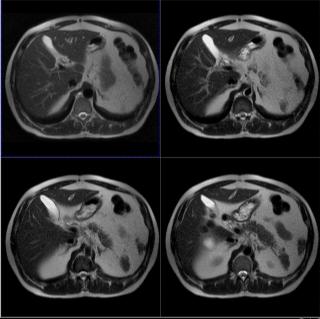
Болезнь Паркинсона — это хроническое и прогрессирующее нейродегенеративное заболевание, которое поражает центральную нервную систему, особенно структуры мозга, отвечающие за координацию движений и поддержание мышечного тонуса и возникает из-за гибели нейронов в области мозга, называемой «черная субстанция», которые вырабатывают дофамин — нейромедиатор, играющий ключевую роль в передаче сигналов между клетками мозга. Недостаток дофамина приводит к нарушениям движения, таких как тремор (дрожание) в покое, скованность мышц, замедленность движений и проблемы с балансом.
Ранняя диагностика болезни Паркинсона на данный момент остается сложной задачей для медицинского сообщества и требует комплексного подхода - данных истории болезни, экспертизы врача-невролога и результатов исследования МРТ головного мозга. С ростом продолжительности жизни и неблагоприятной экологической обстановкой все больше жителей Санкт-Петербурга имеют шансы дожить до диагноза Паркинсон. Этот недуг становиться одной из причин роста инвалидности населения в области неврологических заболеваний. Именно поэтому очень важно выявить эту патологию вовремя на ранней стадии развития. Ведь к более адекватному ответу на лечение приводит лишь своевременно начатая терапия. Механизма появления и развития этой патологи до конца еще не открыт. Считается, что это заболевание отчасти зависит от наследственности, а отчасти может быть вызвано триггерными факторами, например, экологической обстановкой.
Основные типы болезни Паркинсона
Болезнь Паркинсона может иметь несколько типов, которые выделяют в зависимости от её причин, особенностей проявления и течения.
Идиопатическая болезнь Паркинсона - это наиболее распространённый тип, при котором точные причины заболевания не установлены. Этот тип, известный также как «классическая» болезнь Паркинсона, проявляется основными симптомами: тремором, ригидностью мышц, нарушением координации и замедленностью движений. Он связан с постепенным разрушением дофаминовых нейронов в мозге, но генетические и экологические факторы также могут играть роль.
Генетический Паркинсонизм. В некоторых случаях заболевание вызвано наследственными мутациями. При этом типе Паркинсона болезнь чаще всего начинается раньше, а её течение может отличаться по выраженности симптомов и скорости прогрессирования. К генам, ассоциированным с этой формой болезни, относятся мутации в генах LRRK2, PARK7, PINK1, SNCA и PRKN.
Атипичные формы паркинсонизма. К атипичным формам паркинсонизма относятся заболевания, схожие по симптомам с болезнью Паркинсона, но имеющие иные причины и патофизиологию:
- Прогрессирующий надъядерный паралич: сопровождается трудностями с движением глаз, падениями, нарушениями равновесия и речевыми нарушениями.
- Кортикобазальная дегенерация: характеризуется мышечной ригидностью, односторонними двигательно-координационными нарушениями и деменцией.
- Множественная системная атрофия: заболевание, поражающее несколько систем организма, вызывает значительные трудности с координацией, проявляется мышечным тремором и другими двигательными нарушениями. Эти типы заболевания обычно менее чувствительны к традиционным методам лечения, используемым при идиопатической форме болезни Паркинсона.
Вторичный (симптоматический) паркинсонизм развивается в результате внешних воздействий, которые вызывают повреждения дофаминовой системы. К основным причинам относят:
- Приём определённых лекарств (например, антипсихотических средств).
- Травмы головы.
- Инфекции головного мозга (например, энцефалит).
- Токсическое воздействие (например, воздействие марганца или угарного газа).
Сосудистый паркинсонизм вызван повреждением сосудов головного мозга (чаще у пожилых людей с сердечно-сосудистыми заболеваниями). В результате нарушения кровоснабжения могут проявляться паркинсонические симптомы, такие как тремор, мышечная ригидность, но они отличаются от классических признаков болезни Паркинсона.
Признаки
Болезнь Паркинсона прогрессирует медленно, и её признаки можно разделить на ранние и поздние. На ранних стадиях симптомы могут быть едва заметны:
- Тремор: слабая дрожь в пальцах или кистях рук, заметная в состоянии покоя.
-
Изменение почерка: почерк становится мелким и неразборчивым.
-
Замедление движений: простые действия, такие как подъём с кресла или ходьба, выполняются медленнее.
-
Нарушение равновесия: нестабильность при ходьбе или стоянии.
-
Маскообразное лицо: сниженная мимическая активность, лицо становится «замороженным».
-
Проблемы со сном: такие как частые пробуждения, беспокойные движения во время сна.
На более поздних стадиях симптомы усиливаются и могут существенно снижать качество жизни:
-
Сильный тремор: дрожь становится более выраженной и может распространяться на обе стороны тела.
-
Выраженная ригидность: сильное напряжение мышц, скованность.
-
Нарушение походки: шаги становятся мелкими и неровными; также может проявляться «прилипающий шаг» или ощущение застывания при попытке начать движение.
-
Сгибательная поза: типичная сутулость, наклонённый вперёд корпус.
-
Проблемы с глотанием и речью: осиплость, затруднения при проглатывании пищи и жидкости.
-
Когнитивные нарушения: снижение памяти, концентрации, развитие деменции.
У пациента могут возникнуть депрессия, тревожность, стойкая усталость, потеря обоняния и проблемы с мочеиспусканием.
Причины
Современные исследования выделяют несколько факторов, которые могут быть связаны с развитием болезни Паркинсона:
Около 15% случаев болезни Паркинсона имеют семейную историю, что указывает на наличие наследственного компонента. Выявлено более десятка генов, связанных с риском заболевания, включая гены LRRK2, SNCA, PARK7, PINK1, и PRKN. Некоторые мутации этих генов увеличивают риск патологии, особенно в случаях раннего начала болезни. Генетические исследования также показывают, что гены, связанные с воспалением, метаболизмом нейротрофических факторов и функцией митохондрий, могут играть ключевую роль в развитии заболевания.
Оксидативный стресс — состояние, при котором в клетках накапливаются свободные радикалы, которые могут повреждать структуры клеток, особенно нейронов. Нарушения в митохондриальной функции, органеллах, ответственных за производство энергии в клетках, также связаны с болезнью Паркинсона. Исследования показывают, что нарушения в митохондриальной активности могут способствовать гибели дофаминовых нейронов в головном мозге, особенно в области, отвечающей за координацию движений.
Современные исследования обнаруживают, что хроническое воспаление может быть одним из факторов, способствующих разрушению нейронов при болезни Паркинсона. При этом в головном мозге наблюдается активность микроглии — клеток, отвечающих за иммунный ответ. Хроническая активация микроглии может повреждать нейроны, увеличивая воспаление и риск нейродегенерации. У пациентов наблюдается повышенная концентрация провоспалительных цитокинов, что указывает на системное воспаление в организме.
Контакт с некоторыми токсинами, такими как пестициды (например, паракват и ротенон), промышленными химикатами и тяжёлыми металлами, связан с повышенным риском болезни Паркинсона. Исследования показывают, что эти вещества могут вызывать повреждение дофаминовых нейронов, особенно в области черной субстанции головного мозга. Заболевание также чаще встречается среди людей, проживающих в сельской местности, что может быть связано с воздействием сельскохозяйственных химикатов.
Болезнь Паркинсона, как правило, развивается у людей старше 60 лет, и риск повышается с возрастом. Старение вызывает снижение способности организма к восстановлению клеток и делает нейроны более уязвимыми к повреждению, что может увеличивать риск нейродегенеративных заболеваний.
Недавние исследования выявили, что кишечная микрофлора может влиять на развитие болезни Паркинсона. Было установлено, что нарушения микробиома могут вызвать хроническое воспаление и даже синтез белка α-синуклеина — ключевого фактора, связанного с развитием болезни. Предполагается, что изменения в микрофлоре могут способствовать патологическим процессам в головном мозге через ось «кишечник-мозг».
Основным белком, участвующим в патогенезе болезни Паркинсона, является α-синуклеин. В норме он присутствует в клетках, но при патологии начинает скапливаться и образует токсические кластеры (лейви-тельца), что повреждает нейроны. Нарушения в системе переработки клеточного «мусора», особенно в лизосомах, также связывают с болезнью. Генетические мутации и возраст могут ухудшать эту функцию, что ведёт к накоплению повреждённых белков.
Методы диагностики болезни Паркинсона
Основные методы диагностики при болезни Паркинсона включают:
- Магнитно-резонансная томография (МРТ) используется для исключения других заболеваний, таких как опухоли или сосудистые патологии головного мозга, которые могут вызывать симптомы, схожие с болезнью Паркинсона. МРТ помогает оценить состояние структур мозга, но не всегда даёт чёткие признаки болезни Паркинсона.
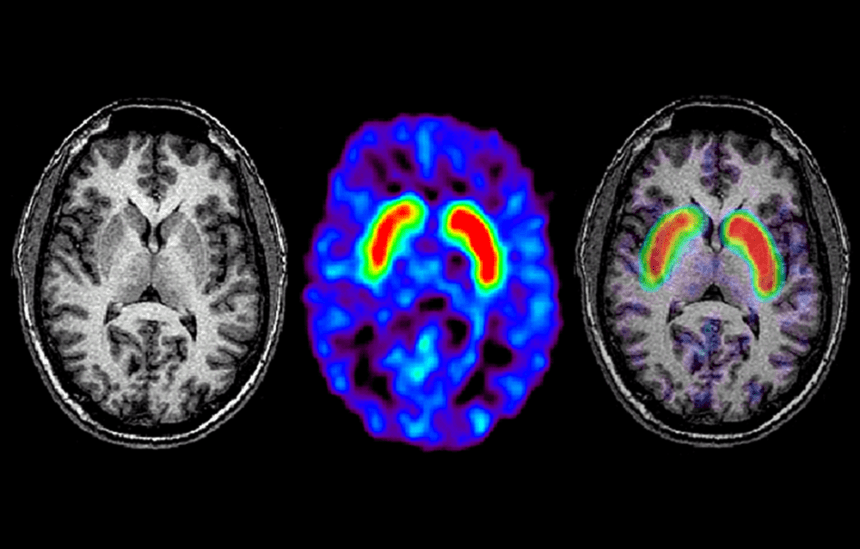
- Позитронно-эмиссионная томография (ПЭТ) применяется для оценки метаболической активности мозга, позволяя выявить снижение дофаминовой активности в базальных ганглиях, что характерно для болезни Паркинсона и помогает подтвердить диагноз на ранних стадиях.
- Электроэнцефалография (ЭЭГ) используется для оценки электрической активности головного мозга, позволяя исключить эпилептические расстройства или другие заболевания, сопровождающиеся изменениями в активности мозга, хотя специфических изменений при болезни Паркинсона на ЭЭГ обычно не выявляется.
- Реоэнцефалография (РЭГ) применяется для оценки кровоснабжения мозга и выявления сосудистых нарушений, которые могут сопровождать или усугублять течение болезни Паркинсона, что важно для дифференциальной диагностики и выбора тактики лечения.
- Функциональные нейровизуализационные методы, такие как однофотонная эмиссионная компьютерная томография (ОФЭКТ), позволяют выявить снижение уровня дофамина в черной субстанции мозга, что является специфическим признаком болезни Паркинсона и помогает в ранней диагностике заболевания.
- Нейропсихологическое тестирование проводится для оценки когнитивных функций, таких как память, внимание и исполнительные функции, которые могут страдать при прогрессировании болезни Паркинсона, что позволяет оценить степень когнитивных нарушений и их влияние на качество жизни пациента.
Диагностика этого недуга инструментальными методами при помощи КТ или МРТ головы, а также ПЭТ - это сложная задача, поскольку прямых и точных признаков болезни Паркинсона пока не выявлено. Если выбирать из современных методов диагностики, то сейчас набирает силу метод позитронно-эмиссионной томографии, на котором при подозрении на болезнь Паркинсона исследование проводится с применением флуородопа. Недостатком данного исследования является его низкая доступность даже в таких крупных городах и очень дорогостоящая диагностика.
Основной диагностический недостаток ПЭТ заключается в том, что в ходе сканирования используются радиоактивные препараты, и не всегда получается анатомически точно локализовать найденный патологический очаг. Поэтому в медицинских центрах СПб наиболее распространенной формой аппаратной диагностики при болезни Паркинсона является МРТ головного мозга, которая более доступна широкому кругу пациентов.
Что показывает МРТ при болезни Паркинсона
 В диагностике болезни Паркинсона очень важен правильный сбор анамнеза, особенно информации о том, как развивалось заболевание, какие симптомы появились первично. Врачу необходимо установить, есть ли у пациента такие важные признаки, как:
В диагностике болезни Паркинсона очень важен правильный сбор анамнеза, особенно информации о том, как развивалось заболевание, какие симптомы появились первично. Врачу необходимо установить, есть ли у пациента такие важные признаки, как:
- олигобрадикинезия;
- ригидность мышц;
- постуральная неустойчивость;
- развитие депрессии на фоне изменений состояния пациента.
Перед неврологом стоит задача определить и другие симптомы, которые могут говорить о каких-то других заболеваниях. Для этого врачи часто назначают сделать МРТ головного мозга при подозрении на болезнь Паркинсона. Она позволяет оценить состояние черной субстанции вещества головного мозга и провести дифференциальную диагностику для исключения следующих патологий:
- демиелинизация;
- новообразования;
- возрастные дегенеративные изменения головного мозга.
МРТ головного мозга при Паркинсоне
МРТ головного мозга при Паркинсоне следует сделать на высокопольном аппарате с напряженностью магнитного поля 1.5 Тесла и выше. Такое обследование, как правило, проходит без контраста и позволяет визуализировать очаги поражения черной субстанции мозга. Особой подготовки данное сканирование не требует, однако характерный для больных Паркинсоном тремор может создать некоторые диагностические сложности. Высокопольный томограф очень чувствителен к любому движению. Оно может смазать изображения на получаемых в ходе процедуры снимках. Длительность МРТ головы обычно составляет 15-20 минут, и пациент все это время должен лежать неподвижно. Иногда больным Паркинсона на поздних стадиях заболевания такая неподвижность дается с трудом.
МРТ ночью
Ночные цены в Санкт-Петербурге
Болезнь Паркинсона МРТ признаки
Для дифференциальной диагностики болезни Паркинсона в медицинских центрах используют протокол - МРТ головного мозга в SWI-режиме (в режиме изображений, взвешенных по магнитной восприимчивости). Такая МРТ показывает не только признаки вторичного паркинсонизма, но и визуализирует типичные для этой болезни изменения черной субстанции (отсутствие нигросомы-1) при первичной форме заболевания. Изображение не поврежденных тканей мозга в середине черной субстанции напоминает хвост ласточки. А вот у больных болезнью Паркинсона данное разделение на две доли исчезает.
Снижение объёма черной субстанции в среднем мозге, что визуализируется как уменьшение интенсивности сигнала в области черной субстанции, хотя это не всегда ярко выражено на стандартных МРТ изображениях, особенно на ранних стадиях болезни.
Признаки атрофии в базальных ганглиях и других структурах, связанных с моторной функцией, которые могут проявляться в виде уменьшения объема тканей в этих областях, что связано с прогрессированием болезни и длительной потерей нейронов.
Отсутствие или минимальные изменения в коре головного мозга, что помогает исключить другие дегенеративные заболевания, такие как болезнь Альцгеймера или сосудистые деменции, при которых на МРТ наблюдаются более выраженные корковые изменения.
Сужение внутренней капсулы мозга, что может быть косвенным признаком длительных дегенеративных изменений, связанных с моторной дисфункцией, хотя такие изменения наблюдаются на более поздних стадиях.
Отсутствие значимых структурных изменений на ранних стадиях болезни Паркинсона, что важно для дифференциальной диагностики, так как МРТ в основном используется для исключения других патологий, вызывающих схожие симптомы (опухоли, сосудистые заболевания).
Что покажет ЭЭГ при болезни Паркинсона
ЭЭГ при болезни Паркинсона обычно не выявляет специфических признаков, характерных только для данного заболевания, но могут наблюдаться следующие изменения:
- Уменьшение альфа-ритма, что проявляется снижением частоты и амплитуды альфа-ритмических волн, особенно в задних отделах головного мозга, что свидетельствует о нарушениях в когнитивных функциях и активности мозга, которые могут возникать при прогрессировании болезни.
- Замедление электрической активности мозга, что проявляется увеличением дельта- и тета-активности, особенно у пациентов с более выраженными когнитивными нарушениями или деменцией, которая иногда сопровождает поздние стадии болезни Паркинсона.
- Нарушение межполушарной симметрии, которое может наблюдаться как асимметричное распределение ритмов и активности, что связано с поражением подкорковых структур и базальных ганглиев.
- Отсутствие эпилептиформной активности, что помогает исключить эпилепсию или другие формы судорожных расстройств, которые могут маскировать симптомы, схожие с болезнью Паркинсона.
Что покажет реоэнцефалография при болезни Паркинсона
Реоэнцефалография при болезни Паркинсона выявляет следующие характерные признаки:
- Снижение тонуса мозговых артерий, что проявляется как уменьшение амплитуды пульсовых колебаний на реоэнцефалограмме, что может указывать на сосудистые нарушения и ухудшение кровоснабжения мозга, особенно в зонах, связанных с моторной функцией.
- Затруднение венозного оттока, которое выявляется как удлинение времени ретроградной волны на графике, что может свидетельствовать о венозном застое и нарушении оттока крови из мозга, что иногда сопровождает нейродегенеративные заболевания, включая болезнь Паркинсона.
- Снижение скорости кровотока в артериях мозга, что проявляется в виде замедления фаз кровенаполнения, что может указывать на сосудистую недостаточность, связанную с ухудшением регуляции мозгового кровообращения.
- Нарушение эластичности сосудов, что выражается в изменении кривой РЭГ, свидетельствующее о повышенной ригидности артериальных стенок, что может сопровождаться снижением их адаптивности к изменению кровяного давления, особенно у пожилых пациентов.
- Ассиметрия кровообращения между полушариями, которая выявляется как различия в амплитуде или фазах на графике РЭГ, что может свидетельствовать о локализованных нарушениях кровоснабжения в базальных ганглиях или других моторных центрах.
Список литературы:
- Артемьев Д.В. Возрастные аспекты болезни Паркинсона. // Болезнь Паркинсона и расстройство движений: Руководство для врачей по материалам II Национального конгресса. Москва 21-23 сентября 2011г. М., 2011: с. 59-62.
- Захаров В.В., Ярославцева Н.В., Яхно Н.Н. Когнитивные нарушения при болезни Паркинсона. // Неврологический журнал 2003; №2: с.11-16.
- Иллариошкин С. Н. Паркинсонизм с ранним началом. // Атмосфера: Нервные болезни 2006; №3: с. 14-20.
- Левин О.С. Федорова Н.В. Болезнь Паркинсона. // М., 2006. 256 с.
- Левин О.С. Диагностика и лечение депрессии при болезни Паркинсона. // Атмосфера: Нервные болезни 2006; №6: с. 2-8
- Caviness J.N., LihFen Lue, Adler Ch.H. et al. Parkinson's Disease Dementia and Potential Therapeutic Strategies. // CNS Neuroscience & Therapeutics 2011; vol. 17: p. 32 -44
- Gerhard A., Brooks D.J. PET and SPECT Imaging in Atypical Parkinsonian Disorders. In: Litvan I. (eds) Atypical Parkinsonial disorders. // Totowa, New Jersey: Humana Press, 2005: p. 459-471
- Huber S.J., Shuttelworth E.C., Christy J.A. et al. Magnetic resonance imaging in dementia of Parkinson's disease. // Journal of Neurology, Neurosurgery, and Psychiatry 1989; vol.52: p. 1221-1227
Прогрессирующий надъядерный паралич (альтернативное название прогрессирующий супрануклеарный паралич) - это дегенерирующие заболевание.
МРТ сосудов мозга и головы - это комплексное обследование как вещества и оболочек головного мозга, так и его сосудистого русла. Такое комплексное исследование можно сделать в любом МРТ центре СПб, и включает оно два сканирования, которые проходят друг за другом: МРТ головного мозга; МРТ сосудов головного мозга (она же МРТ ангиография сосудов головного мозга).
Головной мозг в медицинских центрах СПб можно обследовать с помощью КТ и МРТ, а что лучше выбрать, об этом мы поговорим в этой статье. Если образно описывать диагностическую разницу между этими двумя томографиями, то компьютерная томография - это истребитель, который быстро несется по всем областям тела, а МРТ - это вертолет, который садится и проводит точные и скрупулезное обследование какой-то конкретной области.
 Служба бесплатной
Служба бесплатной